高校化学の問題演習
アルキン
※鳥取大学の入試問題です。(化学式については、たとえば、CO2はCO2などのように、原子数の数字はそのまま元素記号の後に入力すること)
次の文を読み、以下の問いに答えよ。
アセチレンは、石油を高温で分解してつくられる。また、炭化カルシウム(カーバイド)に水を加えてつくることもできる。
アセチレンは ア 反応を起こしやすい。例えば、白金やニッケルを触媒としてアセチレンに水素を反応させると、 イ を経て ウ になる。また、臭素水中の臭素もアセチレンに対して ア 反応を起こす。この他にも、水銀(Ⅱ)イオンを触媒として、希硫酸中でアセチレンと水を反応させると A が生成するが、これもまたアセチレンへの ア 反応の例である。ただし、 A は不安定で、すぐに B に変わる。この方法は B の主要な工業的製法であったが、水銀公害の問題が生じたため、その後は使われていない。現在は イ を酸素で酸化して B が製造されている。
問1 下線部の反応を化学反応式で書け。(矢印以外はすべて半角で入力すること。また、化学反応式の両辺は炭素原子を含んでいる物質ではじめること。)
問2 文中の ア ~ ウ にあてはまる語句を、以下の語群から選んで書け。
語群:
置換,付加,脱水,縮合,重合,
メタン,エタン,プロパン,
エチレン,プロペン,1-ブテン,
ベンゼン,エタノール,ポリエチレン,
塩化ビニル,ポリ塩化ビニル
問3 文中の A と B にあてはまる化合物名とその構造式を書け。
結晶格子
※( )内の年度のセンター試験の問題を参考に作られています。(答えはすべて半角数字で入力すること)
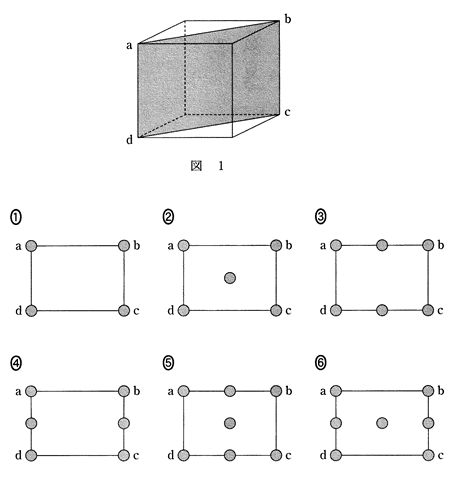
問1 図1は面心立方格子の金属結晶の単位格子を示している。この単位格子の頂点a,b,c,dを含む面に存在する原子の配置を表す図として正しいものを、下の①~⑥のうちから一つ選べ。ただし、●は原子の位置を表している。
(2016(平成28))
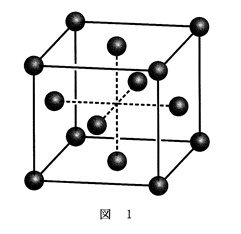
問2 図1のような面心立方格子の結晶構造をもつ金属の原子半径を$r$〔cm〕とする。この金属結晶の単位格子一辺の長さ$a$〔cm〕を表す式として最も適当なものを、下の①~⑥のうちから一つ選べ。
(2017(平成29))
① \( \displaystyle \frac{4\sqrt{3}}{3}r \) ② \( 2\sqrt{2}r \)
③ $4r$ ④ \( \displaystyle \frac{2\sqrt{3}}{3}r \)
⑤ \( \sqrt{2}r \) ⑥ $2r$
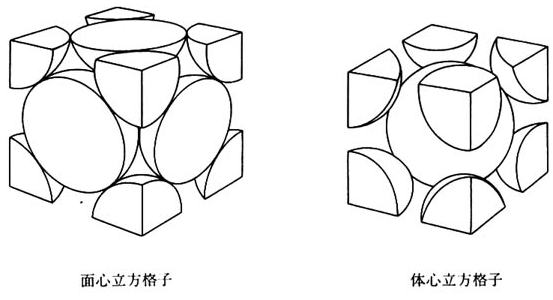
問3 同じ大きさの球を用いて、面心立方格子と体心立方格子をつくった。図は、それぞれの格子の、配列の最小単位(単位格子)を示したものである。次の記述①~⑤のうちから、正しいものを一つ選べ。
(1997(平成9))
① 面心立方格子の方が、体心立方格子よりも単位格子内に含まれる球の数が多い。
② 面心立方格子と体心立方格子では、単位格子の一辺の長さが等しい。
③ 面心立方格子と体心立方格子では、一つの球に接する球の数が等しい。
④ 面心立方格子よりも体心立方格子の方が、同じ体積で比べると球が密に詰め込まれている。
⑤ 面心立方格子と体心立方格子は、ともに単位格子の中心に隙間がない。
混合物の燃焼
※愛知工業大学の入試問題です。
メタノールとエタノールとの混合物がある。これを完全燃焼させたところ、二酸化炭素2.64gと水(液体)1.98gを得た。このときに必要な酸素の体積は標準状態で何Lか。有効数字2桁で答えよ。$\ce{H}$ = 1.0,$\ce{C}$ = 12,$\ce{O}$ = 16
立体異性体
※( )内の年度のセンター試験の問題を参考に作られています。
| a | b | c | d | |
| ① | 正 | 正 | 正 | 正 |
| ② | 正 | 正 | 誤 | 正 |
| ③ | 正 | 誤 | 正 | 誤 |
| ④ | 正 | 誤 | 誤 | 誤 |
| ⑤ | 誤 | 正 | 正 | 誤 |
| ⑥ | 誤 | 正 | 誤 | 誤 |
| ⑦ | 誤 | 誤 | 正 | 正 |
| ⑧ | 誤 | 誤 | 誤 | 正 |
問1 互いに鏡像の関係にある一対の光学異性体に関する次の記述a~dについて、正誤の組合せとして正しいものを、右の①~⑧のうちから一つ選べ(答えは半角数字で入力すること)。
(2001(平成13))
a 偏光(平面偏光)に対する性質が異なる。
b 融点・沸点が異なる。
c 立体構造が異なる。
d 分子式が異なる。
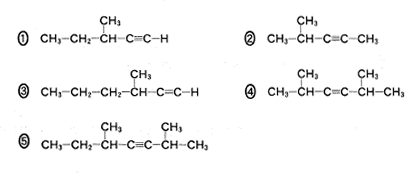
問2 次の記述(ア・イ)が両方ともに当てはまる化合物の構造式として最も適当なものを、下の①~⑤のうちから一つ選べ(答えは半角数字で入力すること)。
(2011(平成23))
ア 水素1分子が付加した生成物には、幾何異性体(シス-トランス異性体)が存在する。
イ 水素2分子が付加した生成物には、不斉炭素原子が存在する。
化学結合
※立命館大学の入試問題を参考に作られています。
次の文中の〔 A 〕~〔 F 〕に入れる適当な語句を下記の語群より選べ。また、X,Yには元素記号を、Zには電子式を記せ。
(記号については全角カタカナのみ、元素記号については半角アルファベットのみで入力すること)
陽イオンと陰イオンの静電気的引力による原子間の結合を〔 A 〕結合という。2個の原子がそれぞれ不対電子を出しあって〔 B 〕をつくり、結合する場合を〔 C 〕結合という。このような結合をしている原子の電子配置は、〔 D 〕原子の電子配置と同じになる。例えば、$\ce{H2O}$の$\ce{H}$原子は X 原子と同じ電子配置になり、$\ce{O}$原子は Y 原子と同じ電子配置になる。$\ce{H2O}$は電子式で Z と表される。
特定の原子に固定されず、多数の原子間を移動している価電子を〔 E 〕電子とよび、これを多数の原子が共有してできる化学結合を〔 F 〕結合という。
(ア)配位 (イ)共有 (ウ)共有電子対
(エ)非共有電子対 (オ)自由 (カ)イオン
(キ)金属 (ク)アルカリ金属 (ケ)陽
(コ)陰 (サ)正 (シ)負
(ス)ハロゲン (セ)希ガス (ソ)水素
