高校化学の問題演習
ハロゲンの性質
※岩手大学の入試問題を参考に作られています。
次の文章を読み、問1~問3に答えよ。
塩素などの17族の元素は( ア )と呼ばれる。( ア )の原子は、( イ )を7個持ち、電子を受け入れて、( ウ )価の( エ )イオンになりやすい。
単体の( ア )は、いずれも有色、有毒であり、分子全体として( オ )のかたよりのない無極性分子である。これらは、常温常圧において気体、液体、固体として存在し、他の物質から電子を奪う力が強い。
( ア )の水素化合物は、すべて強い刺激臭を持ち、室温で無色の気体であり、水によく溶け、酸性を示す。これらの水溶液には、①ガラス容器に保存できないものがある。
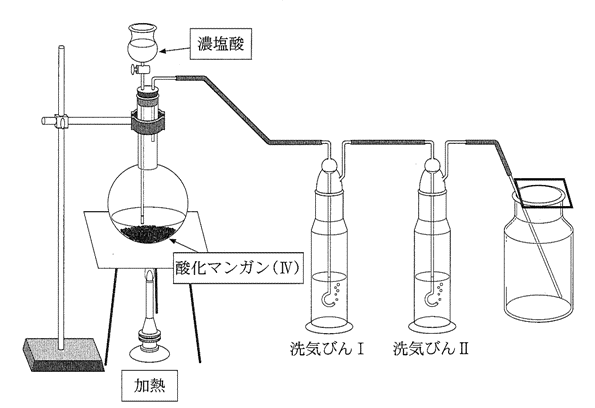
単体の塩素は、図に示す装置を用いて、②酸化マンガン(Ⅳ)に濃塩酸を加えて加熱し、発生する気体を洗気びんに通して捕集すると得られる。工業的には、塩化ナトリウム水溶液の電気分解によって製造される。
問1 文章中の( ア )~( オ )に適切な用語または数値を書け。(数値は半角数字で入力すること)
問2 下線①に当てはまる( ア )の水素化合物の水溶液の名称を答えよ。また、ガラス容器に保存できない理由を40字以内で述べよ。
問3 以下の設問(1)~設問(3)に答えよ。
(1) 下線②の化学反応式を書け。
(2) 図中の洗気びんⅠおよび洗気びんⅡの液体の名称を書き、それぞれの液体の役割とそれらを用いる理由を述べよ。
(3) 図のような塩素の捕集方法を何と呼ぶか。その名称を答えよ。(漢字4字で答えること)
酸化剤・還元剤
※( )内の年度のセンター試験の問題を参考に作られています。
問1 下線で示す物質が還元剤としてはたらいている化学反応の式を、次の①~⑥のうちから一つ選べ(答えは半角数字で入力すること)。
(2011(平成23))
① $\small{\ce{2\underline{H2O} + 2K -> 2KOH + H2 }}$
② $\small{\ce{\underline{Cl2} + 2KBr -> 2KCl + Br2 }}$
③ $\small{\ce{\underline{H2O2} + 2KI + H2SO4 -> 2H2O + I2 + K2SO4 }}$
④ $\small{\ce{\underline{H2O2} + SO2 -> H2SO4 }}$
⑤ $\small{\ce{\underline{SO2} + Br2 + 2H2O -> H2SO4 + 2HBr }}$
⑥ $\small{\ce{\underline{SO2} + 2H2S -> 3S + 2H2O }}$
問2 次の酸化還元反応ア~エのうち、下線を引いた物質が酸化剤としてはたらいているものはいくつあるか。その数を下の①~⑤のうちから一つ選べ(答えは半角数字で入力すること)。
(2013(平成25))
ア $\small{\ce{\underline{Cu} + 2H2SO4 -> CuSO4 + SO2 + 2H2O }}$
イ $\small{\ce{\underline{SnCl2} + Zn -> Sn + ZnCl2 }}$
ウ $\small{\ce{\underline{Br2} + 2KI -> 2KBr + I2 }}$
エ $\small{\ce{2\underline{KMnO4} + 5H2O2 + 3H2SO4 -> 2MnSO4 + 5O2 + K2SO4 + 8H2O }}$
ア
$\small{\ce{\underline{Cu} + 2H2SO4 -> CuSO4 + SO2 + 2H2O }}$
イ
$\small{\ce{\underline{SnCl2} + Zn -> Sn + ZnCl2 }}$
ウ
$\small{\ce{\underline{Br2} + 2KI -> 2KBr + I2 }}$
エ
$\small{\ce{2\underline{KMnO4} + 5H2O2 + 3H2SO4 \\ -> 2MnSO4 + 5O2 + K2SO4 + 8H2O }}$
① 1 ② 2 ③ 3
④ 4 ⑤ 0
物質の成り立ち
※上智大学の入試問題を参考に作られています。
次の文章を読み、問に答えよ。
私たちの身の回りにある多くの物質は、2種類以上の物質が混じり合ったものであり、このような物質を( A )という。空気や海水は( A )である。これに対して、他の物質が混じっていない単一の物質を( B )という。( B )には、1種類の元素からなる( C )と、2種類以上の元素からなる( D )とがある。同じ元素の( C )で性質の異なるものを互いに( E )であるという。
問 文中の( A )~( E )にあてはまる語句をa)~s)からそれぞれ1つ選べ。
a)異性体 b)化合物 c)希釈 d)揮発
e)凝縮 f)原子 g)コロイド h)混合物
i)重合体 j)純物質 k)蒸留 l)精製
m)単体 n)単量体 o)同位体 p)同族体
q)同素体 r)複塩 s)沸騰
合成高分子
次の文章を読んで、あとの問いに答えなさい。
合成高分子でできている素材は数多くある。たとえば、6,6-ナイロンはカルボン酸の( A )とアミンの( B )から合成されている。清涼飲料水のボトルや繊維として多量に使われている( C )は、芳香族の( D )と( E )から合成されている。
(1)( C )に入る語句を答えなさい。
(2)6,6-ナイロンや( C )の物質が合成されるための重合反応は何重合とよばれているか答えなさい。
(3)( A )、( B )、( D )、( E )にあてはまる物質の構造式を書きなさい。
濃度平衡定数
$\ce{H2 + I2 <=> 2HI}$の反応について、次の問いに答えなさい。
(1)$T$〔K〕で$\ce{H2}$、$\ce{I2}$を2.0mol/l入れたところ、平衡状態で0.50mol/lの$\ce{I2}$が残った。平衡定数$K$を求めなさい。(半角数字で入力すること)
(2)$T$〔K〕で$\ce{H2}$2.0mol/l、$\ce{I2}$2.0mol/l、$\ce{HI}$4.0mol/lを入れたとき、反応ははじめ右左のどちらに進むか答えなさい。また、平衡状態でのそれぞれのモル濃度も求めなさい。(モル濃度は半角数字で入力すること)
